Сердечная недостаточность со сниженной фракцией выброса (СНнФВ) является основным типом сердечной недостаточности. Китайское исследование СН показало, что 42% сердечных недостаточностей в Китае связаны с СНнФВ, хотя для лечения СНнФВ доступно несколько стандартных терапевтических классов препаратов, которые снижают риск. случаев смерти и госпитализации по поводу сердечной недостаточности в той или иной степени. Тем не менее, пациенты подвергаются высокому риску рецидива сердечной недостаточности, усугубляющего события, смертность остается на уровне около 25%, а прогноз остается плохим. Таким образом, по-прежнему существует острая потребность в новых терапевтических средствах для лечения СНнФВ, а Верицигуат, новый стимулятор растворимой гуанилатциклазы (рГЦ), изучался в исследовании VICTORIA, чтобы оценить, может ли Верицигуат улучшить прогноз пациентов с СНнФВ. Исследование представляет собой многоцентровое рандомизированное плацебо-контролируемое двойное слепое событийно-ориентированное исследование III фазы клинических исходов в параллельных группах. В исследовании, проведенном под эгидой Центра VIGOR в Канаде в сотрудничестве с Институтом клинических исследований Дьюка, приняли участие 616 центров в 42 странах и регионах, включая Европу, Японию, Китай и США. Наше кардиологическое отделение имело честь принять участие. Всего обследовано 5050 пациентов с хронической сердечной недостаточностью в возрасте ≥18 лет, II-IV класса по NYHA, ФВ <45%, с повышенным уровнем натрийуретического пептида (NT-proBNP) в течение 30 дней до рандомизации, госпитализированных по поводу сердечной недостаточности. в течение 6 месяцев до рандомизации или получали диуретики внутривенно по поводу сердечной недостаточности в течение 3 месяцев до рандомизации, были включены в исследование, все получали ESC, AHA/ACC и национальные/региональные руководства рекомендуют стандарт лечения. Пациенты были рандомизированы в соотношении 1:1 на две группы и получилиВерисигуат(n=2526) и плацебо (n=2524) в дополнение к стандартной терапии соответственно.
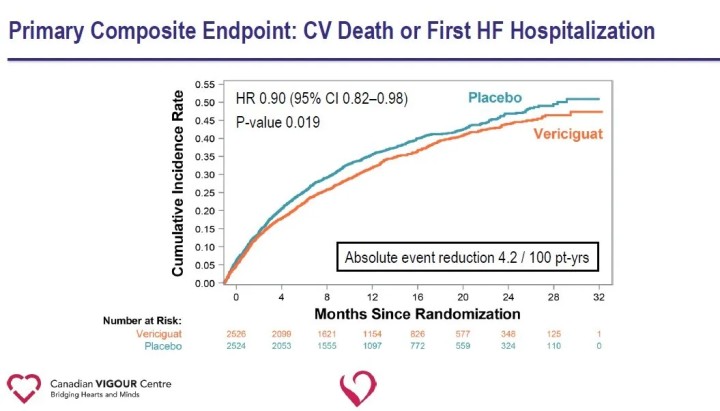
Первичной конечной точкой исследования была комбинированная конечная точка: смерть от сердечно-сосудистых заболеваний или первая госпитализация по поводу сердечной недостаточности; вторичные конечные точки включали компоненты первичной конечной точки, первую и последующие госпитализации по поводу сердечной недостаточности (первые и повторные события), составную конечную точку - смерть по любой причине или госпитализацию по поводу сердечной недостаточности, а также смерть по любой причине. При медиане наблюдения 10,8 месяцев наблюдалось относительное 10%-ное снижение первичной конечной точки сердечно-сосудистой смерти или первой госпитализации по поводу сердечной недостаточности в группе Верицигуата по сравнению с группой плацебо.
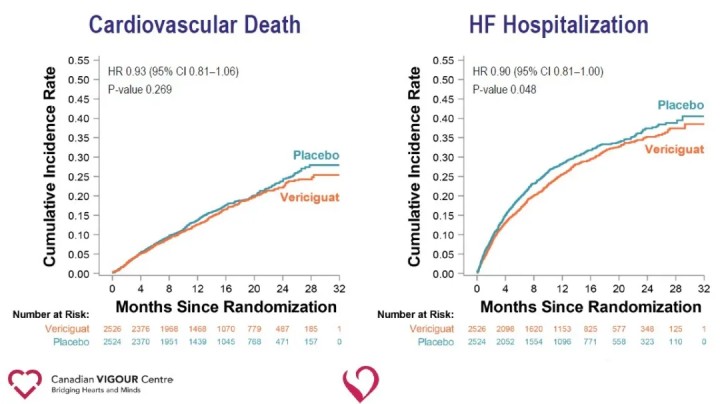
Анализ вторичных конечных точек показал значительное снижение частоты госпитализаций по поводу сердечной недостаточности (ОР 0,90) и значительное снижение комбинированной конечной точки смерти от всех причин или госпитализации по поводу сердечной недостаточности (ОР 0,90) в группе Верицигуата по сравнению с группой плацебо.
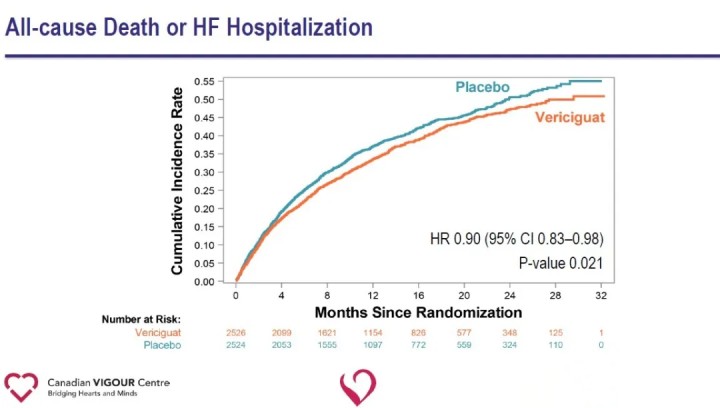
Результаты исследования показывают, что добавлениеВерисигуатСтандартное лечение сердечной недостаточности значительно снижает недавнее возникновение ухудшения событий сердечной недостаточности и снижает риск комбинированной конечной точки сердечно-сосудистой смерти или госпитализации по поводу сердечной недостаточности у пациентов с СНнФВ. Способность Верицигуата снижать риск комбинированной конечной точки сердечно-сосудистой смерти или госпитализации по поводу сердечной недостаточности у пациентов с сердечной недостаточностью высокого риска открывает новые терапевтические возможности при сердечной недостаточности и открывает новые пути для будущих исследований сердечно-сосудистых заболеваний. Верицигуат в настоящее время не одобрен для продажи. Безопасность, эффективность и экономическая эффективность препарата все еще нуждаются в дальнейшем тестировании на рынке.
Время публикации: 09 февраля 2022 г.
